CENTRE DE RÉFÉRENCE
PRÉSENTATION
Nous avons le plaisir de vous annoncer que le centre de référence maladies rares « Syndrome Néphrotique Idiopathique de l’Enfant et de l’Adulte » crée en 2006 a été de nouveau labellisé suite à l’évaluation d’un jury mandaté par la DGOS (arrêté ministériel du 9 Mai 2017).
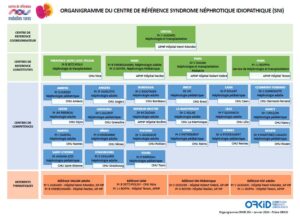
Vous trouverez le nouvel organigramme du centre de référence dans l’onglet « Equipe » (site coordonnateur, sites constitutifs et centres de compétence).
Comme vous le verrez nous avons souhaité que des référents par thématiques (SNI de l’enfant, SNI de l’adulte et GEM) puissent animer les différentes missions pour lesquelles le CRMR a été créé.
Durant cette nouvelle mandature, nous souhaitons pouvoir poursuivre les travaux initiés depuis plus de 10 ans dans les domaines du parcours de soins, de l’expertise, du médico-social et de l’éducation thérapeutique.
Nous espérons que dans l’avenir notre CRMR pourra susciter de nouvelles vocations pour nos jeunes collègues dans le domaine du SNI et des GEM.
Très Cordialement
Coordonnateur du CRMR SNI de l’enfant et de l’adulte
Vincent Audard (Hôpital Henri Mondor)
Référents SNI de l’adulte
Bertrand Knebelmann (Hôpital Necker enfants malades)
Emmanuelle Plaisier (Hôpital Tenon)
Dil Sahali (Hôpital Henri Mondor)
Référents SNI de l’enfant
Olivia Boyer (Hôpital Necker enfants malades)
Claire Dossier (Hôpital Robert Debré)
Référents GEM
Vincent Esnault (CHU de Nice)
Pierre Ronco (Hôpital Tenon)
MISSIONS
Une part importante du travail effectué depuis 10 ans a consisté à rédiger des PNDS (Protocole National de Diagnostic et de Soins) qui seront dans les années qui viennent de nouveau actualisés en prenant en compte les avancées diagnostiques et thérapeutiques majeures concernant le SNI et les GEM.
Dans le domaine de la recherche clinique et translationnelle, nous souhaitons organiser chaque année une réunion scientifique au cours de laquelle les néphrologues adultes et pédiatres qui le souhaitent pourront présenter leur projet de recherche. Nous souhaitons pouvoir répondre de manière collective avec votre aide aux appels d’offres nationaux et internationaux (via notamment la participation des sites constitutifs au réseau européen des maladies rénales rares ERKNet).
Nous souhaitons développer nos actions en concertation et à l’interface avec le réseau ERKNet, qui apporte une dimension internationale à nos actions dont l’importance dans l’harmonisation des pratiques et la mise en œuvre d’actions concertées de recherche est évidente.
Le CRMR a développé depuis sa création des relations privilégiées avec l’association de patients atteints de SNI que nous souhaitons voir perdurer.
Dans les années qui viennent, un travail important va nous être demandé dans le cadre de la surveillance épidémiologique des maladies rénales rares. Avec l’aide de la filière ORKID (qui hébergera désormais notre site internet), nous allons veiller à rendre possible et le plus exhaustif possible le travail de recensement des cas de SNI et GEM dans les bases de données maladie rares.
La BNDMR (Banque Nationale de Données Maladies Rares) est une base de données nationale qui vise à documenter le parcours des patients atteints de maladies rares dans les centres experts. Elle permettra de mieux évaluer l’impact des plans nationaux et de suivre la prise en charge et l’état de santé des patients par pathologie.
Nous souhaitons que notre CRMR puisse être pour les patients, les médecins et les chercheurs un lieu de rencontres, d’échanges conviviaux et constructifs et de confrontations permettant de participer activement à l’amélioration des connaissances de la pathogénie du SNI et des GEM, et d’améliorer la prise en charge globale des patients.
EQUIPE
Afin d’optimiser et homogénéiser la prise en charge du SNI et des GEM sur l’ensemble du territoire, un référent néphrologue adulte et un référent néphrologue pédiatre ont été identifiés dans l’ensemble des centres de compétences. Ces référents participeront à la réunion scientifique annuelle du CRMR SNI et seront des relais indispensables dans le domaine de la recherche et du soin.
Organigramme du centre de référence SNI
TROMBINOSCOPE
- Hôpital Henri Mondor
- Hôpital Necker
- CHU de Nice
- Hôpital Tenon
 Pr Vincent AUDARD (Néphrologue adulte) Coordonnateur CRMR Syndrome Néphrotique Idiopathique
Pr Vincent AUDARD (Néphrologue adulte) Coordonnateur CRMR Syndrome Néphrotique Idiopathique
Coordonnateur du centre Syndrome Néphrotique Idiopathique de l’enfant et de l’adulte depuis Mai 2017, V Audard est professeur de Néphrologie à l’Université Paris Est Créteil (service de Néphrologie et Transplantation CHU Henri Mondor). Son activité clinique est dédiée à la prise en charge des maladies rénales chroniques et notamment des patients présentant des glomérulopathies. Son activité de recherche (Institut de Mondor de recherche biomédicale équipe 21 INSERM U955, CHU Henri Mondor) porte sur le Syndrome Néphrotique Idiopathique et les Syndromes Néphrotiques secondaires à des maladies hématologiques (Drépanocytose, Hémopathie). V Audard est membre élu du conseil d’administration de la SFNDT et membre du conseil scientifique de la filière de santé maladies rénales rares « Orphan Kidney Diseases » (ORKID).
 Dr Olivia BOYER (Néphrologue pédiatre)
Dr Olivia BOYER (Néphrologue pédiatre)Olivia Boyer est Néphrologue pédiatre à l’hôpital Necker Enfants Malades et enseignante à l’Université Paris Descartes, Sorbonne Paris Cité. Ses travaux de recherche menés à l’Institut Imagine portent principalement sur les maladies rénales rares (syndrome néphrotique, syndrome hémolytique et urémique, polykystose …) et cherchent à mieux comprendre les mécanismes physiopathologiques et génétiques qui les sous-tendent afin de développer des thérapies innovantes ciblées.
 Pr Bertrand KNEBELMANN (Néphrologue Adulte)
Pr Bertrand KNEBELMANN (Néphrologue Adulte)Le Pr Bertrand KNEBELMANN est néphrologue au sein du service de néphrologie-dialyse adulte de l’Hôpital Necker à Paris et Professeur à l’université Paris Descartes. Il est responsable du site constitutif du CMR Syndrome Néphrotique Idiopathique à Necker. Il est également responsable « Adultes » du Centre de Référence Maladies Rénales Héréditaires de l’enfant et de l’Adulte (MARHEA), membre du conseil scientifique de la filière de santé maladies rénales rares « Orphan Kidney Diseases » (ORKID), membre du Conseil scientifique de l’AIRG France (Association pour l’information et la recherche sur les maladies rénales génétiques) ainsi que du Conseil Scientifique de la Société Francophone de dialyse et Transplantation (SFNDT). Son activité clinique porte sur les maladies rénales génétiques et les syndromes néphrotiques et il effectue des consultations de transition vers le centre de Néphrologie Adultes pour les enfants suivis en néphrologie pédiatrique. Ses recherches portent sur plusieurs maladies rénales génétiques et la physiopathologie du SNI.
 Pr Vincent ESNAULT (Néphrologue adulte)
Pr Vincent ESNAULT (Néphrologue adulte)Vincent Esnault est coordinateur du site du CHU de Nice du Centre de Référence Maladie Rare Syndrome Néphrotique Idiopathique. Il est professeur de Néphrologie et chef du service de Néphrologie-Dialyse-Transplantation du CHU de Nice. Son activité clinique est dédiée à la prise en charge des maladies rénales chroniques et notamment des patients présentant des glomérulopathies. Le site de Nice plus spécifiquement impliqué sur le volet Glomérulonéphrite Extra-membraneuse du CRMR fédère sur cette thématique outre le service de Néphrologie-Dialyse-Transplantation, le laboratoire d’Immunologie, le laboratoire d’anatomopathologie, l’unité de Néphrologie pédiatrique du CHU de Nice et l’UMR-CNRS 7275, IPMC, Valbonne Sophia-Antipolis.
 Dr Barbara SEITZ-POLSKI (Néphrologue adulte)
Dr Barbara SEITZ-POLSKI (Néphrologue adulte)
Barbara Seitz-Polski est immunologiste et néphrologue, enseignante à l’Université de Nice Sophia-Antipolis. Elle est responsable de l’unité de consultation du site du CHU de Nice du Centre de Référence Maladie Rare Syndrome Néphrotique Idiopathique au sein du service de Néphrologie-Dialyse-Transplantation. Son activité clinique est principalement dédiée à la prise en charge des glomérulonéphrites extra-membraneuses. Son activité de biologiste se fait au laboratoire d’Immunologie du CHU de Nice et sa recherche sur la physiopathologie des glomérulonéphrites extra-membraneuse se fait en lien avec l’UMR-CNRS 7275, IPMC, Valbonne Sophia-Antipolis et porte sur l’identification de nouveaux marqueurs diagnostiques et pronostiques et le développement de stratégies thérapeutiques innovantes.
 Pr Jean-Jacques BOFFA (Néphrologue adulte) Centre Constitutif – CRMR Syndrome Néphrotique Idiopathique
Pr Jean-Jacques BOFFA (Néphrologue adulte) Centre Constitutif – CRMR Syndrome Néphrotique Idiopathique
Jean-Jacques BOFFA est responsable du Secteur d’hospitalisation conventionnelle de Néphrologie Adulte à l’Hôpital Tenon, et travaille dans l’unité INSERM UMRS 1155. Son activité clinique est notamment centrée sur la prise en charge diagnostique et thérapeutique des patients adultes présentant un syndrome néphrotique de causes variées. Il est l’investigateur principal d’une étude ancillaire de Néphrovir3 intitulée « Valeur diagnostique de l’expression leucocytaire d’isthmine-1 des syndromes néphrotiques idiopathiques de l’enfant et de l’adulte ». Cette étude a pour objectif de démontrer l’intérêt d’un nouveau marqueur découvert pour distinguer les syndromes néphrotiques idiopathiques et HSF primitives des autres causes de syndromes néphrotiques. Son activité de recherche a pour objectifs de comprendre le rôle de l’Isthmine-1 dans la physiopathologie du syndrome néphrotique idiopathique et la hyalinose segmentaire et focale primitive et de déterminer l’intérêt thérapeutique de son inhibition. Il encadre et forme de jeunes chercheurs et médecins.
Dr Karine DAHAN (Néphrologue adulte) Centre Constitutif – CRMR Syndrome Néphrotique Idiopathique
 Karine Dahan est Médecin dans le Service Hôpital de Jour Néphrologie Adulte à l’Hôpital Tenon. Son activité clinique est notamment centrée sur la prise en charge diagnostique et thérapeutique des patients présentant une glomérulonéphrite extra membraneuse (GEM) primitive et des patients présentant un syndrome néphrotique idiopathique. K. Dahan assure une activité de recherche clinique évaluant la prise en charge des patients présentant une GEM. Elle est l’investigateur principal de GEMRITUX, un essai clinique randomisé national financé par un PHRC évaluant l’efficacité du Rituximab dans la glomérulonéphrite extra membraneuse. Elle fait partie des investigateurs de l’étude Eurenomics, étude observationnelle européenne sur la GEM.
Karine Dahan est Médecin dans le Service Hôpital de Jour Néphrologie Adulte à l’Hôpital Tenon. Son activité clinique est notamment centrée sur la prise en charge diagnostique et thérapeutique des patients présentant une glomérulonéphrite extra membraneuse (GEM) primitive et des patients présentant un syndrome néphrotique idiopathique. K. Dahan assure une activité de recherche clinique évaluant la prise en charge des patients présentant une GEM. Elle est l’investigateur principal de GEMRITUX, un essai clinique randomisé national financé par un PHRC évaluant l’efficacité du Rituximab dans la glomérulonéphrite extra membraneuse. Elle fait partie des investigateurs de l’étude Eurenomics, étude observationnelle européenne sur la GEM.
 Margaux REHEL
Margaux REHEL
Infirmière de coordination en recherche clinique et éducation thérapeutique à mi-temps sur CRMR MARHEA et CRMR SNI et mi-temps CRMR maladies respiratoires rares à l’Hôpital TENON, 4 rue de la Chine, 75020 PARIS. Margaux s’occupe de l’inclusion et du suivi en recherche clinique maladies rares et de la coordination bio banque et collection biologique multiples. Référente transition des patients porteurs d’un SNI, en collaboration avec l’hôpital Robert Debré elle est également en lien avec les collaborateurs extérieurs
Virginie AVELLINO
Attachée de Recherche Clinique sur les CRMR MARHEA et CRMR SNI
Le Syndrome Néphrotique Idiopathique
Les reins permettent, grâce aux glomérules, sortes de filtre ou d’«usines de tri des déchets», d’éliminer certains composants présents dans le sang et provenant surtout de l’alimentation, tels l’eau, le sel, l’urée venant des protéines présentes dans la viande ou les produits laitiers.
Ce filtre est très sélectif et ne laisse pas passer certaines substances comme les protéines fabriquées par l’organisme.
Un syndrome néphrotique survient lorsque ce filtre est trop perméable et que les reins laissent passer dans les urines de grandes quantités de protéines présentes dans la circulation sanguine, surtout de l’albumine.
Il en résulte une diminution de la concentration d’albumine dans le sang et une difficulté des reins à éliminer le sel et l’eau provenant de l’alimentation. L’eau et le sel vont passer de la circulation sanguine dans les tissus et provoquer des œdèmes.
Chez l’enfant, le syndrome néphrotique est le plus souvent en rapport avec ce que l’on appelle un syndrome néphrotique idiopathique (dont on ne connaît pas la cause), également appelé néphrose. On distingue deux formes de syndrome néphrotique idiopathique en fonction de la réponse au traitement. Le syndrome néphrotique est dit corticorésistant lorsque le traitement standard du syndrome néphrotique par la cortisone (prednisone) ne permet pas d’obtenir une rémission complète c’est à dire de rendre le filtre de nouveau imperméable aux protéines et de faire disparaître les protéines dans les urines. Le syndrome néphrotique est dit corticorésistant lorsque le traitement standard par la cortisone (prednisone) ne permet pas d’obtenir une rémission complète c’est à dire de rendre le filtre de nouveau imperméable aux protéines et de faire disparaître les protéines dans les urines. Il est dit héréditaire lorsqu’il résulte du dysfonctionnement d’un gène. Le syndrome néphrotique est dit congénital lorsqu’il débute en anténatal ou dans les 3 premiers mois de vie.
La glomérulonéphrite extramembraneuse
Qu’est-ce que la glomérulonéphrite extramembraneuse ?
Les reins contiennent des glomérules qui filtrent le sang, fonctionnant comme des passoires, en retenant les substances de grandes tailles (les protéines et les cellules sanguines) et en laissant passer les déchets, petites substances provenant surtout de l’alimentation, comme l’eau, le sel, l’urée. Ces déchets filtrés se retrouvent alors dans l’urine.
Un syndrome néphrotique survient lorsque les trous de la passoire s’élargissent laissant passer dans les urines des protéines (protéinurie), essentiellement de l’albumine (albuminurie). Il en résulte une diminution de la concentration d’albumine dans le sang qui assure normalement par un effet « éponge » le maintien de l’eau et du sel dans le sang. L’eau et le sel vont donc passer de la circulation sanguine dans les tissus et provoquer des œdèmes.
La glomérulonéphrite extramembraneuse (GEM) est la cause la plus fréquente de syndrome néphrotique de l’adulte à partir de 50 ans. Elle est caractérisée par la mise en évidence sur une biopsie du rein de dépôts granuleux d’anticorps sur le versant externe du filtre, expliquant le terme « extramembraneux ».
En savoir plus
Recommendations vaccinales et syndrome néphrotique idiopathique
Retrouvez ci dessous une présentation sur le travail réalisé par le réseau SNIF concernant les recommandations vaccinales et le syndrome néphrotique idiopathique.
Présentation

Le CRMR SNI reçoit une subvention pour la constitution d’une banque nationale de données et de ressources biologiques de patients atteints de SN acquis
Le centre de référence maladie rare Syndrome Néphrotique Idiopathique de l’Enfant et de l’Adulte a reçu lors du douzième Gala de la Fondation du Rein la subvention de recherche intitulée « Réseau de recherche Syndrome néphrotique acquis » attribuée par la Fondation du Rein et la Fondation Dassault.
PUBLICATIONS
Publications des sites constitutifs CRMR Syndrome Néphrotique Idiopathique (SNI) de l’enfant et de l’adulte sur la thématique du SNI 2012-2018.
- Necker
- Henri Mondor
- Tenon
- Robert Debré
- Nice
1. Gonçalves S, Patat J, Guida MC, (…) Boyer O, (…) Antignac C, Simons M. Correction: A homozygous KAT2B variant modulates the clinical phenotype of ADD3 deficiency in humans and flies. PLoS Genet. 2018 Oct 26;14(10):e1007748. doi: 10.1371/journal.pgen.1007748. eCollection 2018 Oct. PubMed PMID: 30365502.
2. Gribouval O, Boyer O, Hummel A, (…) Tête MJ, Heidet L, Antignac C, Servais A. Identification of genetic causes for sporadic steroid-resistant nephrotic syndrome in adults.Kidney Int. 2018 Nov;94(5):1013-1022. doi: 10.1016/j.kint.2018.07.024. PubMed PMID: 30348286.
3. Gribouval O, Boyer O, Knebelmann B, Karras A, Dantal J, Fourrage C, Alibeu O, Hogan J, Dossier C, Tête MJ, Antignac C, Servais A. APOL1 risk genotype in European steroid-resistant nephrotic syndrome and/or focal segmental glomerulosclerosis patients of different African ancestries.Nephrol Dial Transplant. 2018 Jul 9. doi: 10.1093/ndt/gfy176. PubMed PMID: 29992269.
4. Gonçalves S, Patat J, Guida MC, Lachaussée N, Arrondel C, Helmstädter M, Boyer O, Gribouval O, Gubler MC, Mollet G, Rio M, Charbit M, Bole-Feysot C, Nitschke P, Huber TB, Wheeler PG, Haynes D, Juusola J, Billette de Villemeur T, Nava C, Afenjar A, Keren B, Bodmer R, Antignac C, Simons M. A homozygous KAT2B variant modulates the clinical phenotype of ADD3 deficiency in humans and flies. PLoS Genet. 2018 May 16;14(5):e1007386. doi: 10.1371/journal.pgen.1007386. eCollection 2018 May. Erratum in: PLoS Genet. 2018 Oct 26;14(10):e1007748. PubMed PMID: 29768408; PubMed Central PMCID: PMC5973622.
5. Bérody S, Heidet L, Gribouval O, Harambat J, Niaudet P, Baudouin V, Bacchetta J, Boudaillez B, Dehennault M, de Parscau L, Dunand O, Flodrops H, Fila M, Garnier A, Louillet F, Macher MA, May A, Merieau E, Monceaux F, Pietrement C, Rousset-Rouvière C, Roussey G, Taque S, Tenenbaum J, Ulinski T, Vieux R, Zaloszyc A, Morinière V, Salomon R, Boyer O. Treatment and outcome of congenital nephrotic syndrome.
Nephrol Dial Transplant. 2018 Feb 20. doi: 10.1093/ndt/gfy015. PubMed PMID: 29474669
1. Kormann R, Jannot AS, Narjoz C, Ribeil JA, Manceau S, Delville M, Joste V, Prié D, Pouchot J, Thervet E, Courbebaisse M, Arlet JB. Roles of APOL1 G1 and G2 variants in sickle cell disease patients: kidney is the main target. Br J Haematol. 2017 Oct;179(2):323-335.
2. Garrouste C, Canaud G, Büchler M, Rivalan J, Colosio C, Martinez F, Aniort J, Dudreuilh C, Pereira B, Caillard S, Philipponnet C, Anglicheau D, Heng AE.
Rituximab for Recurrence of Primary Focal Segmental Glomerulosclerosis After Kidney Transplantation: Clinical Outcomes. Transplantation. 2017 Mar;101(3):649-656.
3. Dahan K, Debiec H, Plaisier E, Cachanado M, Rousseau A, Wakselman L, Michel PA, Mihout F, Dussol B, Matignon M, Mousson C, Simon T, Ronco P; GEMRITUX Study Group.. Rituximab for Severe Membranous Nephropathy: A 6-Month Trial with Extended Follow-Up. J Am Soc Nephrol. 2017 Jan;28(1):348-358
4. Baye E, Gallazzini M, Delville M, Legendre C, Terzi F, Canaud G. The costimulatory receptor B7-1 is not induced in injured podocytes. Kidney Int. 2016
Nov;90(5):1037-1044
5. Delville M, Baye E, Durrbach A, Audard V, Kofman T, Braun L, Olagne J, Nguyen C, Deschênes G, Moulin B, Delahousse M, Kesler-Roussey G, Beaudreuil S, Martinez F, Rabant M, Grimbert P, Gallazzini M, Terzi F, Legendre C, Canaud G. B7-1 Blockade Does Not Improve Post-Transplant Nephrotic Syndrome Caused by Recurrent FSGS. J Am Soc Nephrol. 2016 Aug;27(8):2520-7.
1. Minimal change nephrotic syndrome in patients infected with human immunodeficiency virus: a retrospective study of 8 cases. Arrestier R, Satie AP, Zhang SY, Plaisier E, Isnard-Bagnis C, Gatault P, Raimbourg Q, Buob D, Vocila F, Heng AE, Francois H, Moktefi A, Canaud G, Matignon M, Dejucq-Rainsford N, Brocheriou I, Sahali D, Audard V.BMC Nephrol. 2018 ;19(1):331
2. An open-label randomized controlled trial of low-dose corticosteroid plus enteric-coated mycophenolate sodium versus standard corticosteroid treatment for minimal change nephrotic syndrome in adults (MSN Study).
Rémy P, Audard V, Natella PA, Pelle G, Dussol B, Leray-Moragues H, Vigneau C, Bouachi K, Dantal J, Vrigneaud L, Karras A, Pourcine F, Gatault P, Grimbert P, Ait Sahlia N, Moktefi A, Daugas E, Rigothier C, Bastuji-Garin S, Sahali D; MSN Trial Investigators. Kidney Int. 2018 ;94(6):1217-1226
3. NEPHRUTIX: A randomized, double-blind, placebo vs Rituximab-controlled trial assessing T-cell subset changes in Minimal Change Nephrotic Syndrome. Boumediene A, Vachin P, Sendeyo K, Oniszczuk J, Zhang SY, Henique C, Pawlak A, Audard V, Ollero M, Guigonis V, Sahali D. J Autoimmun. 2018 Mar;88:91-102
4. Current insights about recurrence of glomerular diseases after renal transplantation.Kofman T, Oniszczuk J, Lang P, Grimbert P, Audard V. Nephrol Ther. 2018 May;14(3):179-188.
1. Wang HY, Cui Z, Xie LJ, Zhang LJ, Pei ZY, Chen FJ, Qu Z, Huang J, Zhang YM,Wang X, Wang F, Meng LQ, Cheng XY, Liu G, Zhou XJ, Zhang H, Debiec H, Ronco P, Zhao MH. HLA class II alleles differing by a single amino acid associate withclinical phenotype and outcome in patients with primary membranous nephropathy. Kidney Int. 2018 Nov;94(5):974-982. doi: 10.1016/j.kint.2018.06.005. Epub 2018 Aug 30. PubMed PMID: 30173899.
2.Dahan K, Gillion V, Johanet C, Debiec H, Ronco P. The Role of PLA2R Antibody in Treatment of Membranous Nephropathy. Kidney Int Rep. 2017 Nov 3;3(2):498-501. doi: 10.1016/j.ekir.2017.10.013. eCollection 2018 Mar. PubMed PMID: 29725656; PubMed Central PMCID: PMC5932125
3.Berchtold L, Zanetta G, Dahan K, Mihout F, Peltier J, Guerrot D, Brochériou I, Ronco P, Debiec H. Efficacy and Safety of Rituximab in Hepatitis B Virus-Associated PLA2R-Positive Membranous Nephropathy. Kidney Int Rep. 2017 Sep 21;3(2):486-491. doi: 10.1016/j.ekir.2017.09.009. eCollection 2018 Mar. PubMed PMID: 29725654; PubMed Central PMCID: PMC5932116.
4. Van de Logt AE, Dahan K, Rousseau A, van der Molen R, Debiec H, Ronco P, Wetzels J. Immunological remission in PLA2R-antibody-associated membranous nephropathy: cyclophosphamide versus rituximab. Kidney Int. 2018 Apr;93(4):1016-1017. doi: 10.1016/j.kint.2017.12.019. PubMed PMID: 29571438.
5. Li J, Cui Z, Long J, Huang W, Wang J, Zhang H, Wang H, Zhang L, Ronco P, Zhao MH. Primary glomerular nephropathy among hospitalized patients in a national database in China. Nephrol Dial Transplant. 2018 Mar 2. doi: 10.1093/ndt/gfy022. PubMed PMID: 29509919.
1. Lescure FX, Flateau C, Pacanowski J, Brocheriou I, Rondeau E, Girard PM, Ronco P, Pialoux G, Plaisier E. HIV-associated kidney glomerular diseases: changes with time and HAART. Nephrol Dial Transplant. 2012 Jun;27(6):2349-55. doi: 10.1093/ndt/gfr676.
1. Okpechi IG, Ameh OI, Bello AK, Ronco P, Swanepoel CR, Kengne AP. Epidemiology of Histologically Proven Glomerulonephritis in Africa: A Systematic Review and Meta-Analysis. PLoS One. 2016 Mar 24;11(3):e0152203. doi: 10.1371/journal.pone.0152203.
2. Kimura Y, Miura N, Debiec H, Morita H, Yamada H, Banno S, Ronco P, Imai H. Circulating antibodies to α-enolase and phospholipase A(2) receptor and composition of glomerular deposits in Japanese patients with primary or secondary membranous nephropathy. Clin Exp Nephrol. 2017 Feb;21(1):117-126. doi: 10.1007/s10157-016-1235-2.
3. Kofman T, Zhang SY, Copie-Bergman C, Moktefi A, Raimbourg Q, Francois H, Karras A, Plaisier E, Painchart B, Favre G, Bertrand D, Gyan E, Souid M, Roos-Weil D, Desvaux D, Grimbert P, Haioun C, Lang P, Sahali D, Audard V. Minimal change nephrotic syndrome associated with non-Hodgkin lymphoid disorders: a retrospective study of 18 cases. Medicine (Baltimore). 2014 Nov;93(24):350-8. doi: 10.1097/MD.0000000000000206.
4. Smeets B, Stucker F, Wetzels J, Brocheriou I, Ronco P, Gröne HJ, D’Agati V, Fogo AB, van Kuppevelt TH, Fischer HP, Boor P, Floege J, Ostendorf T, Moeller MJ. Detection of activated parietal epithelial cells on the glomerular tuft distinguishes early focal segmental glomerulosclerosis from minimal change disease. Am J Pathol. 2014 Dec;184(12):3239-48. doi: 10.1016/j.ajpath.2014.08.007.
5. Munyentwali H, Bouachi K, Audard V, Remy P, Lang P, Mojaat R, Deschênes G, Ronco PM, Plaisier EM, Dahan KY. Rituximab is an efficient and safe treatment in adults with steroid-dependent minimal change disease. Kidney Int. 2013 Mar;83(3):511-6. doi: 10.1038/ki.2012.444.
1.Debiec H, Dossier C, Letouzé E, Gillies CE, Vivarelli M, Putler RK, Ars E, Jacqz-Aigrain E, Elie V, Colucci M, Debette S, Amouyel P, Elalaoui SC, Sefiani A, Dubois V, Simon T, Kretzler M, Ballarin J, Emma F, Sampson MG, Deschênes G, RONCO P. Transethnic, Genome-Wide Analysis Reveals Immune-Related Risk Alleles and Phenotypic Correlates in Pediatric Steroid-Sensitive Nephrotic Syndrome. J Am Soc Nephrol. 2018 Jul;29(7):2000-2013. doi: 10.1681/ASN.2017111185. Epub 2018 Jun 14.PubMed PMID: 29903748; PubMed Central PMCID: PMC605094
2.Dorval G, Gribouval O, Martinez-Barquero V, Machuca E, Tête MJ, Baudouin V, Benoit S, Chabchoub I, Champion G, Chauveau D, Chehade H, Chouchane C, Cloarec S, Cochat P, Dahan K, Dantal J, Delmas Y, Deschênes G, Dolhem P, Durand D, Ekinci Z, El Karoui K, Fischbach M, Grunfeld JP, Guigonis V, Hachicha M, Hogan J, Hourmant M, Hummel A, Kamar N, Krummel T, Lacombe D, Llanas B, Mesnard L, Mohsin N, Niaudet P, Nivet H, Parvex P, Pietrement C, de Pontual L, Noble CP, Ribes D, Ronco P, Rondeau E, Sallee M, Tsimaratos M, Ulinski T, Salomon R, Antignac C, Boyer O. Clinical and genetic heterogeneity in familial steroid-sensitive nephrotic syndrome. Pediatr Nephrol. 2018 Mar;33(3):473-483. doi:10.1007/s00467-017-3819-9. Epub 2017 Oct 23. PubMed PMID: 29058154.
1. Remission of proteinuria in multidrug-resistant idiopathic nephrotic syndrome following immunoglobulin immunoadsorption. Nattes E, Karaa D, Dehoux L, Peuchmaur M, Kwon T, Deschênes G.Acta Paediatr. 2018 Sep 19. doi: 10.1111/apa.14582.
2. Effect of different rituximab regimens on B cell depletion and time to relapse in children with steroid-dependent nephrotic syndrome. Hogan J, Dossier C, Kwon T, Macher MA, Maisin A, Couderc A, Niel O, Baudouin V, Deschênes G. Pediatr Nephrol. 2018 Aug 14. doi: 10.1007/s00467-018-4052-x.
3. Transethnic, Genome-Wide Analysis Reveals Immune-Related Risk Alleles and Phenotypic Correlates in Pediatric Steroid-Sensitive Nephrotic Syndrome. Debiec H, Dossier C, Letouzé E, Gillies CE, Vivarelli M, Putler RK, Ars E, Jacqz-Aigrain E, Elie V, Colucci M, Debette S, Amouyel P, Elalaoui SC, Sefiani A, Dubois V, Simon T, Kretzler M, Ballarin J, Emma F, Sampson MG, Deschênes G, Ronco P.J Am Soc Nephrol. 2018 Jul;29(7):2000-2013
4. Treating the idiopathic nephrotic syndrome: are steroids the answer? Deschênes G, Dossier C, Hogan J.Pediatr Nephrol. 2018 Jun 4.
5. Autoantibodies against podocytic UCHL1 are associated with idiopathic nephrotic syndrome relapses and induce proteinuria in mice. Jamin A, Berthelot L, Couderc A, Chemouny JM, Boedec E, Dehoux L, Abbad L, Dossier C, Daugas E, Monteiro RC, Deschênes G. J Autoimmun. 2018 May;89:149-161.
1. Phospholipase A2 receptor 1 epitope spreading at baseline predicts reduced likelihood of remission of membranous nephropathy. B. Seitz-Polski, H. Debiec, A. Rousseau, K. Dahan, K. Zaghrini, C. Payré, V.L.M. Esnault, G. Lambeau, P. Ronco. J. Am. Soc. Nephrol. 2017 (in press)
2. Anti-phospholipase A2 receptor antibody levels at diagnosis predicts spontaneous remission of idiopathic membranous nephropathy. P. Jullien, B. Seitz Polski, N. Maillard, D. Thibaudin, B. Laurent, E. Ollier, E. Alamartine, G. Lambeau, C. Mariat. Clin. Kidney J. 2017 Apr;10(2):209-214.
3. Glomérulonéphrite extramembraneuse: physiopathologie et histoire naturelle. B. Seitz-Polski, G. Lambeau, V.L.M. Esnault. Nephrol. Ther. 2017, 13 Suppl 1: S75-S81.
4. Epitope spreading of autoantibody response to PLA2R1 associates with poor prognosis in membranous nephropathy. B. Seitz-Polski, G. Dolla, C. Payré, C. Girard, J. Polidori, K. Zorzi, E. Birgy-Barelli, P. Julien, C. Courivaud, T. Krummel, S. Benzaken, G. Bernard, S. Burtey, C. Mariat, V.L.M. Esnault*, G. Lambeau* (* co-last author). J. Am. Soc. Nephrol. 2016, 27: 1517-33.
5. Cross-reactivity of anti-PLA2R1 antibodies to rabbit and mouse PLA2R1 antigens and development of two novel ELISAs with different diagnostic performances in idiopathic membranous nephropathy. B. Seitz-Polski, G. Dolla, C. Payré, N.M. Tomas, M. Lochouarn, L. Jeammet, C. Mariat, T. Krummel, S. Burtey, C. Courivaud, W. Schlumberger, K. Zorzi, S. Benzaken, G. Bernard, V.L.M. Esnault*, G. Lambeau* (* co-last author). Biochimie 2015, 118: 104-15.
CONTACT
Pour répondre au mieux aux attentes des praticiens et des patients, nous avons souhaité créer 3 adresses mails pour les demandes d’avis qui seront directement transférés aux animateurs de chacun des 3 groupes :
- SNI de l’adulte : sni.cdr@aphp.fr
- SNI de l’enfant : pedsni.cdr@aphp.fr
- GEM : gem.cdr@aphp.fr
Référents locaux adultes et pédiatriques